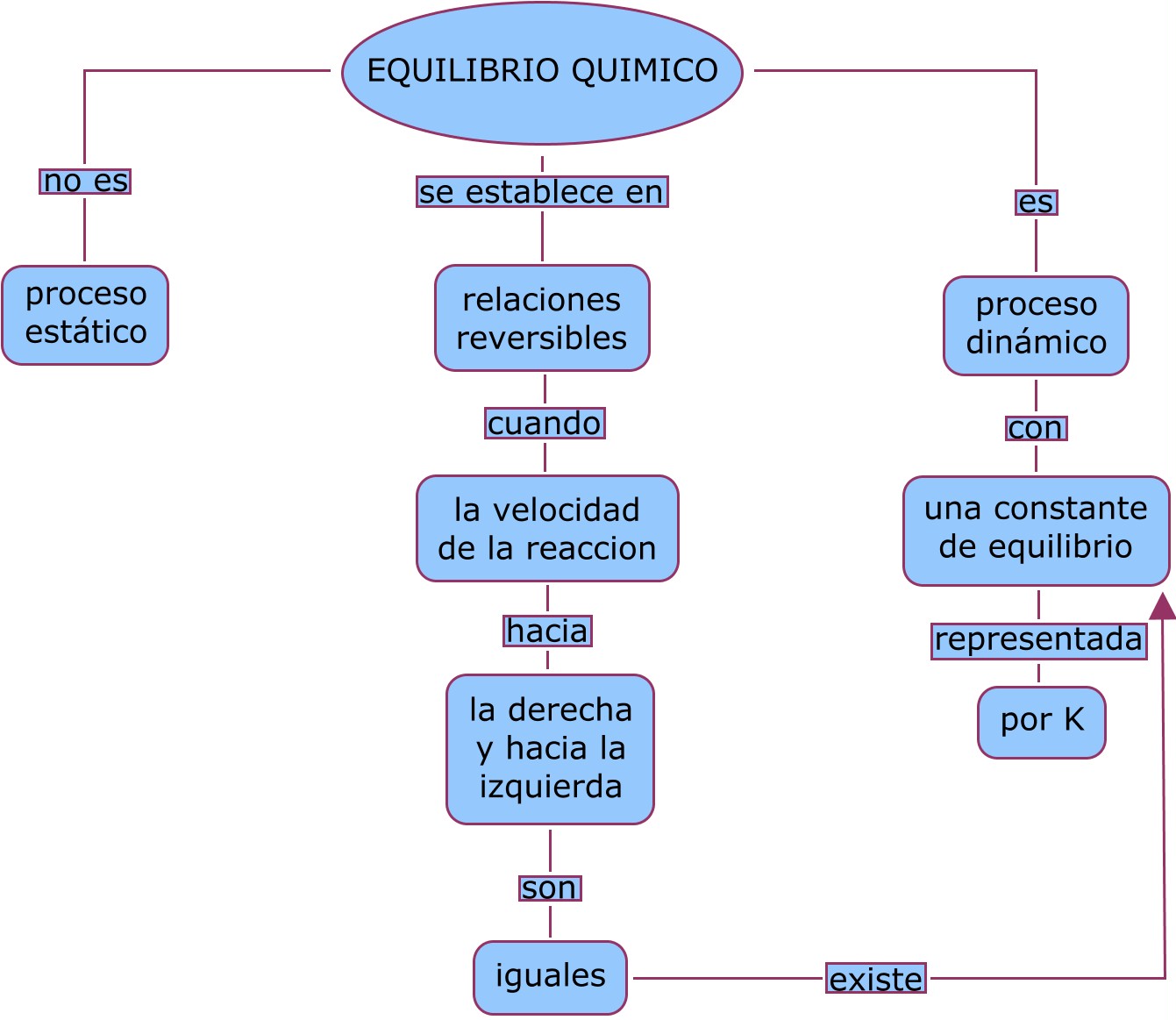
Algunas de las reacciones se producen en su totalidad, es decir, los reactivos se mezclan y no vuelven al estado inicial, pero en otros la reacción puede ser reversible, es en estos casos que se manifiesta el equilibrio químico.
Como ejemplo de reacción irreversible tenemos la combustión, cuando un determinado material es quemado, él nunca vuelve a ser como era antes, es decir, se vuelve cenizas y así permanece. Entonces, ¿qué sería una reacción reversible? Ella ocurre tanto en procesos químicos como en procesos físicos y consiste en la unión de las reacciones directa e inversa.
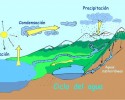
Ejemplo: Si ponemos una cantidad de agua líquida en un recipiente cerrado se da cuenta de que las moléculas de H2O son simultáneamente de estado líquido para el gaseoso y viceversa. Para confirmar que esta afirmación basta con observar que el recipiente que empañado, es decir, el vapor de agua es responsable por este aspecto.
Veamos la ecuación del proceso:
H2O(l) ↔ H2O(v)
La doble flecha indica que la reacción ocurre de la forma directa e inversa, el agua líquida se transforma en vapor, y el vapor se convierte en líquido nuevamente. Siendo así, podemos afirmar que en el sentido directo de la reacción el reactivo líquido forma el producto H2O (v), y en el sentido inverso el producto reacciona para formar H2O (l).
Pero ¿qué relación tiene el equilibrio químico con lo descrito? Antes de eso vamos a recapitular los cambios de estado: en la reacción directa de la ecuación anteriormente señalada tenemos la vaporización (líquido para vapor) y en la reacción inversa tendremos la condensación (vapor para líquido). Entonces podemos decir que en una misma reacción están presentes las velocidades de vaporización y de condensación. El equilibrio químico solamente ocurre cuando estas dos velocidades se igualan:
Velocidad de vaporización ? Velocidad de condensación
El equilibrio químico no es más que la estabilidad entre los productos y los reactivos.