La mayoría de los materiales encontrados en la naturaleza no son sustancias puras, es decir, no se constituyen de un solo tipo de partículas o moléculas; en realidad, son una mezcla compuesta por dos o más sustancias diferentes.
Pero la separación de los componentes de estas mezclas o fraccionamiento de ellos (o incluso su análisis inmediato) son importantes para muchos aspectos de nuestras vidas, cómo separar los contaminantes del agua y convertirla en apta para consumo, en la producción de metales y de componentes especiales que son usados para producir medicamentos, alimentos, bebidas, productos de higiene y limpieza; en la obtención de sal de cocina, en el análisis de los componentes de la sangre en los laboratorios, para separar los componentes de la basura y destinarlos al tratamiento correcto o para reciclaje y así sucesivamente.
Sin embargo, visto que las composiciones varían, para realizar la separación de mezclas, es necesario aplicar métodos especiales o técnicas para cada caso. Las técnicas pueden ser químicas o físicas, porque el principio básico es utilizar las propiedades de los componentes de las mezclas para separarlos. Estas propiedades pueden ser el punto de fusión, el punto de ebullición, la solubilidad, la densidad, entre otros.
Conociendo estas propiedades, entonces podemos determinar si es necesario aplicar solamente uno de los métodos de separación de mezclas o si debemos aplicar múltiples.
Procesos de separación de mezclas
Conozcamos a continuación los principales procesos de separación de mezclas homogéneas y heterogéneas:
Catación: método manual de separación, como cuando escogemos los granos para cocinar.
Ventilación: arrastre por corriente de aire de uno de los componentes de la mezcla que sea bien leve. Ejemplos: separación de las cáscaras de granos de café, cereales y maní tostado.
Levigación: arrastre de sólidos de baja densidad por medio de corrientes de agua, permaneciendo en el recipiente los sólidos de mayor densidad. Eso es hecho, por ejemplo, para separar la arena (menos densa) del oro (más denso).
Tamización: es usada para separar sólidos de diferentes tamaños, generalmente pasando por un colador, y los sólidos más pequeños pasan a través de la malla, siendo separada de los más grandes. Es ampliamente utilizado en la construcción para separar la arena de la grava y en la cocina cuando se quiere separar impurezas en la harina de trigo.
Extracción por solventes: se usa algún líquido para extraer uno o más componentes de la mezcla. Por ejemplo, si añadimos una solución acuosa de cloruro de sodio en una mezcla de gasolina y alcohol, agitamos y después colocamos en reposo, veremos que el agua separa el etano de la gasolina. Eso se basa en la diferencia de polaridad y en el tipo de fuerzas intermoleculares.
El etanol tiene una parte polar y otra apolar, siendo que su parte apolar es atraída por las moléculas de la gasolina, que también son apolares, por la fuerza del dipolo inducido. Pero su parte polar, caracterizada por la presencia del grupo OH, es atraída por las moléculas de agua, que también son polares, realizando enlaces de hidrógeno que son más fuertes que los enlaces del tipo dipolo inducido.
Flotación: la flotación consiste en agregar burbujas de aire en una suspensión coloidal, que, a su vez, está clasificada como un compuesto formado por partículas en suspensión en un líquido, y estas partículas son de entre 1 y 1000 nm. Por ejemplo, en la minería y extracción de cobre a partir de calcopirita (CuFeS2) esta es pulverizada y combinada con aceite, agua y detergente. Después de inyectar aire a través de la mezcla, el sulfato mineral revestido de aceite es atraído por las bolas de aire y es arrastrado para la superficie con la espuma. El residuo no deseado se deposita en la parte inferior.
Filtración: es un método de separación de mezclas heterogéneas de sólido-líquido o gases sólidos que se basa en el pasaje de la mezcla a través de un filtro. Existen dos tipos de filtración: la común y la vacía. La filtración común es el simple paso de la mezcla por un embudo con papel de filtro al vacío donde los sólidos quedan retenidos. Ya la filtración al vacío es hecha usando un embudo Büchner acoplando un kitasato, que, a su vez, está acoplado a una trompa de agua que arrastra el aire dentro del kitasato, causando una región de presión baja. Esa diferencia de presión lleva a la succión del líquido de la mezcla y acelera el proceso de filtración.
Decantación sedimentación, centrifugación y sifonación: estos procesos se basan en un principio único: la diferencia de densidad entre los componentes de la mezcla. Ellos acostumbran a ser usados en conjunto para separar mezclas heterogéneas de dos tipos: líquido + sólido y líquidos inmiscibles.
Este tipo de separación comienza en sedimentación. La mezcla es dejada en reposo para que, después de un tiempo, las partículas del sólido en suspensión en el líquido o el líquido más denso, por acción de la gravedad, se depositen en el fondo del recipiente. Ese proceso de sedimentación puede ser acelerado por la realización de una centrifugación, en el caso de mezclas del tipo líquido + sólido. La mezcla es colocada en un tubo de ensayo dentro de una centrífuga, que gira a alta velocidad y, por inercia, hace que las partículas de mayor densidad se depositen en el fondo del tubo.
La decantación se produce al inclinarse el recipiente que contiene la mezcla, vertiendo en otro recipiente o líquido menos denso, que quedó en la parte superior. Eso puede ser hecho también por sifonación, que es la transferencia del líquido por medio de un sifón o una manguera plástica, iniciándose el flujo de succión.
Separación magnética: es el enfoque de un imán magnético de una mezcla que contiene cualquier sustancia que es atraída por el imán, como las limaduras de hierro, para separarlo de los otros componentes.
Evaporación: esta técnica se basa en la diferencia de puntos de ebullición entre los componentes de la mezcla. Las mezclas homogéneas sólido-líquido, es decir, las soluciones químicas verdaderas, son dejadas en reposo o calentadas para que el líquido evapore, permaneciendo el sólido que posee el punto de ebullición mucho mayor. Esa técnica es usada en la obtención de sal de cocina a partir de agua del mar.
Sin embargo, a través de este método de separación de mezclas, uno de los componentes se pierde. ¿Y si queremos obtener ambos componentes? En este caso, utilizamos la destilación, explicada a continuación:
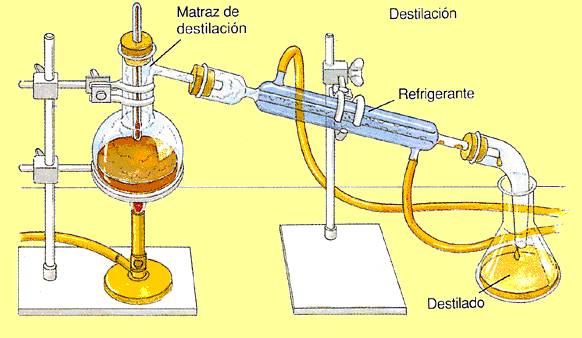
Destilación se utiliza para separar cada componente de la mezcla sólido-líquido o líquido-líquido miscible. Existen dos tipos: destilación simple y destilación fraccionada. La destilación simple se utiliza principalmente para mezclas sólido-líquido y consiste en la mezcla en un matraz de fondo redondo conectada a un condensador de calefacción. El líquido de menor punto de ebullición se evapora y alcanza el condensador, donde vuelve a estado líquido y se recoge en otro recipiente.
Ya la destilación fraccionada se utiliza para mezclas líquido-líquido miscible. La única diferencia es que, antes del condensador, hay una columna de fraccionamiento, en que hay una barrera, pues ese condensador posee bolitas o pedazos de vidrio o de porcelana.
Así, solamente el líquido que tenga menor punto de ebullición conseguirá pasar por la columna de fraccionamiento, mientras el otro sufrirá condensación y volverá para el matraz de destilación.
Cristalización fraccionada: se utiliza cuando hay varios sólidos disueltos en un disolvente y el disolvente se evapora o la temperatura es disminuida. Uno de los componentes comienza a cristalizar, mientras los otros están disueltos. Él es retirado, y el próximo componente se cristaliza y así en adelante.
Licuefacción fraccionada: se utiliza para separar los componentes gaseosos reduciendo la elevación de la temperatura o la presión. Uno de los gases se convierte en líquido en primer lugar, pasando por destilación fraccionada más adelante. Es una técnica empleada para separar los componentes del aire.
Adsorción: sustancias que retienen en sus áreas determinadas sustancias gaseosas se utilizan. Por ejemplo, las máscaras de gas venenoso tienen carbón activo que absorbe los gases contaminantes.
Disolución fraccionada: usada para separar mezclas del tipo sólido-sólido en donde uno de los sólidos se mezcla en determinado solvente y otro no. Por ejemplo, si tenemos una mezcla de sal y arena, podemos añadir agua para que la sal se mezcle en ella y se separe de la arena. Pueden ser usados otros procesos después, como la filtración para separar la arena, la destilación para separar el agua y la sal, o la evaporación para obtener solamente sal.
Fusión fraccionada: método aplicado para separar mezclas de tipo sólido-sólido que tienen diferentes puntos de fusión. La mezcla se calienta y uno de los sólidos se funde primero.