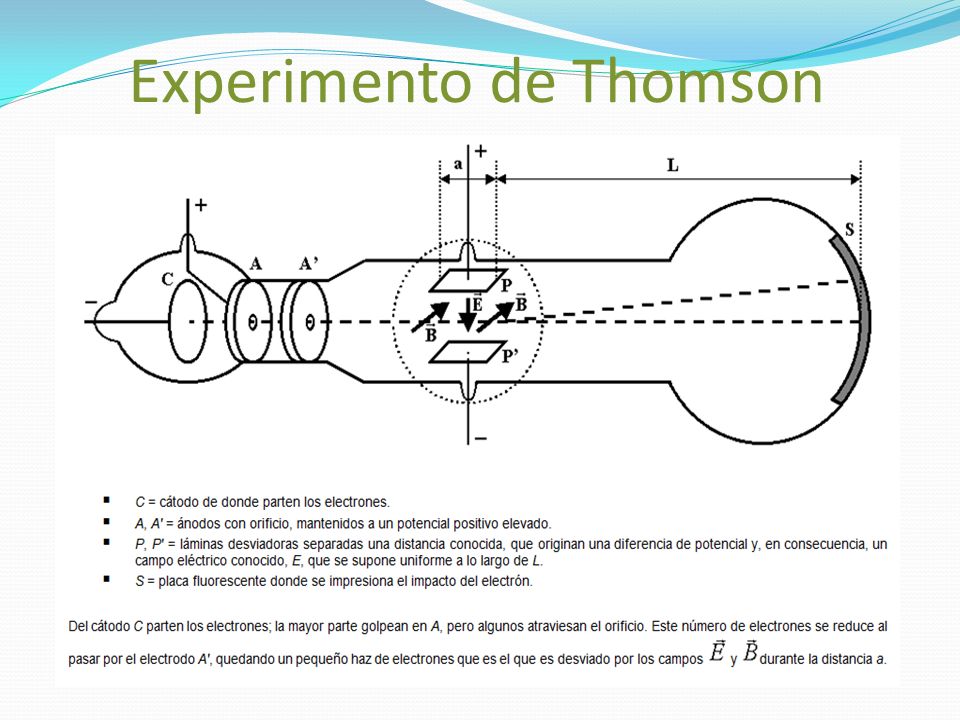
El experimento de Thomson consistió en colocar un campo eléctrico y magnético externo al tubo de Crookes, que retenía gases sometidos a baja presión y electrodos en alta tensión.
El modelo atómico de Thomson argumentó que el átomo era sólido, esférico y divisible, pues era formado por un fluido de carga positiva en el cual estaban dispersas partículas de carga negativa, los electrones. Pero, ¿cómo él descubrió que existían electrones en los átomos? Eso fue posible gracias a un experimento bastante interesante. Veamos de qué se trata:
Thomson realizó su experimento en 1897 y usó como principal herramienta un instrumento conocido como ampolla de Crookes o tubo de rayos catódicos. Este dispositivo fue creado por el físico Inglés William Crookes (1832-1919) en 1856. El tubo de Crookes estaba compuesto por una ampolla de vidrio totalmente sellada. En el interior eran colocados gases bajo baja presión y, en cada extremidad, quedaba un electrodo, es decir, de un lado había un cable de metal unido al polo positivo de una fuente de alta tensión, el ánodo, y de otro había otro metal, llamado de cátodo, que estaba unido al polo negativo.
Al conectar la alta tensión, era posible observar un flujo luminoso saliendo del cátodo y yendo en dirección rectilínea al ánodo. Ese haz pasó a ser llamado de rayo catódico.
El procedimiento realizado por Thomson era básicamente esto: él puso campos eléctricos y magnéticos en la región externa a la ampolla de Crookes y observó que, al ser sometidos a esos campos, los rayos catódicos sufrían un desvío en su trayectoria, yendo en dirección al polo positivo.
Con ese experimento, Thomson realizó tres proposiciones importantes sobre los rayos catódicos:
1. Poseían carga negativa. Dado que esos rayos eran desviados en la dirección del polo positivo, Thomson concluyó que ellos eran constituidos por partículas negativas (cargas opuestas se atraen).
2. Poseían masa. Al colocar una pequeña hélice dentro del tubo, los rayos catódicos se movían, mostrando así que eran partículas con masa.
3. Eran un componente del átomo. Él realizó ese experimento para varios tipos de gases y siempre sucedía lo mismo. Además de eso, los resultados del experimento llevaron a determinar el valor de la relación entre la carga del electrón y su masa (e/m = 1,758805 . 1011 C . kg-1). Thomson observó que ese valor siempre era el mismo y que no dependía de la naturaleza del gas. Así, él constató que aquellas partículas negativas formaban parte de toda materia, es decir, eran parte del átomo.
Y fue así que Thomson descubrió la primera partícula subatómica, el electrón, y, con eso, determinó su modelo atómico.